Notions de base de la spectroscopie Raman
La spectroscopie est l'étude de l'interaction entre la matière et la lumière. Il existe différents types de spectroscopie, qui sont généralement nommés d'après soit la source de lumière utilisée (par exemple, la spectroscopie IR) soit le processus d'interaction lumière-matière exploité. La spectroscopie Raman repose sur la diffusion inélastique de la lumière dans une substance dans laquelle la lumière incidente transfert de l’énergie aux vibrations moléculaires. La lumière diffusée peut être détectée par un spectromètre Raman et représente une « empreinte chimique » de la substance. Sur la base de telles informations spectrales, un matériau peut être identifié ou caractérisé. La spectroscopie Raman appartient au groupe des spectroscopies vibratoires. Cet article présente les principes fondamentaux de la spectroscopie Raman et les bases de la mesure.
Informations liées à la spectroscopie Raman
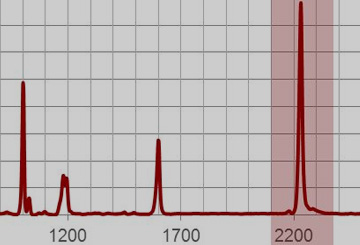
Interprétation des spectres Raman
Obtenir un spectre Raman n'est que le début. Apprenez à interpréter l'image Raman.

Comment la spectroscopie Raman peut-elle vous aider ?
En savoir plus sur le principe de la spectroscopie Raman ainsi que sur les utilisations de la spectroscopie Raman

Spectromètres Raman Instruments pour l'analyse Raman
Comment fonctionne la spectroscopie Raman ?
Comprendre la spectroscopie Raman nécessite des connaissances sur les propriétés de la lumière.
Propriétés de la lumière
La lumière est une forme de radiation électromagnétique, qui a à la fois des propriétés d'onde et de particule ("photon"). Les ondes lumineuses sont généralement décrites mathématiquement par une fonction cosinus, où les deux paramètres caractéristiques les plus importants sont la longueur d'onde (distance entre deux crêtes ou creux d'onde consécutifs) et l'amplitude (hauteur des ondes par rapport à la ligne de base).
Pour une discussion détaillée sur ce sujet, voir "Qu'est-ce que la lumière – une particule ou une onde ?"
La radiation électromagnétique se propage dans l'espace en transportant une certaine quantité d'énergie électromagnétique. Cette énergie est proportionnelle à sa fréquence $\nu$ d'oscillation, qui est reliée à la longueur d'onde $\lambda$ par la vitesse de la lumière $c$ (équation 1) :
$$\nu=\frac{c}{\lambda}$$
Équation 1: $\nu$ = fréquence, $\lambda$ = longueur d'onde, $c$ = vitesse de la lumière
Par conséquent, une onde lumineuse (ou photon) transporte plus d'énergie E plus la fréquence est grande ou, alternativement, plus la longueur d'onde est petite (Équation 2).
$$E ∝ \nu ∝ \frac{1}{\lambda}$$
Équation 2 : $\nu$ = fréquence, $\lambda$ = longueur d'onde, $E$ = énergie
Pour des raisons historiques, les spectroscopistes aiment également utiliser le nombre d'onde $ṽ$, qui est défini comme l'inverse de la longueur d'onde. Le nombre d'onde est directement proportionnel à l'énergie du photon (Équation 3) et généralement exprimé en unités de centimètres réciproques (cm–1) pour donner des chiffres faciles à lire.
$$ṽ=\frac{1}{\lambda}=\frac{\nu}{c}$$
Équation 3: $\nu$ = fréquence, $\lambda$ = longueur d'onde, $c$ = vitesse de la lumière
La description ci-dessus est valable pour une seule onde lumineuse ou photon. Cependant, un faisceau lumineux est composé de nombreuses ondes lumineuses avec des fréquences différentes se propageant dans la même direction. Chaque fréquence contribue au faisceau avec intensité I (c'est-à-dire un certain nombre de photons par intervalle de temps). L'intensité d'un faisceau lumineux est la quantité qui est finalement mesurée avec le détecteur d'un spectromètre. La distribution d'intensité de toutes les fréquences est appelée le spectre de ce faisceau lumineux. Seule une petite partie des fréquences lumineuses peut être vue par l'œil humain ("lumière visible"). D'autres régions spectrales sont par exemple les micro-ondes, l'infrarouge, l'ultraviolet (UV) ou les radiations Röntgen (rayons X) (Figure 2). Pour la spectroscopie Raman, la lumière visible ou la lumière infrarouge (IR) est utilisée pour l'excitation.[1][2][3]
Les paramètres physiques les plus importants et leurs équations correspondantes pertinents pour la spectroscopie Raman sont résumés dans Tableau 1.
Interactions lumière-matière
Lorsqu'un faisceau lumineux frappe la matière, il interagira avec elle d'une manière spécifique, dépendant de l'interaction entre les ondes lumineuses et les atomes et molécules qui composent la matière. L'interaction peut laisser l'énergie de la matière et de la lumière inchangée (par exemple, la réfraction, la réflexion, la diffusion élastique) ou conduire à un échange d'énergie entre les deux. Les procédés utilisés en spectroscopie pour caractériser la matière relèvent de cette dernière catégorie. Le transfert d'énergie de la lumière vers la matière entraîne une excitation. La section suivante décrit les processus d'excitation les plus importants nécessaires pour comprendre la spectroscopie Raman : absorption, fluorescence et diffusion.[3]
Absorption
L'énergie lumineuse dans certaines parties du spectre électromagnétique est (partiellement) transférée à la matière. Cela signifie que certaines ondes lumineuses traversent la matière sans modification (transmission), tandis que certaines lumières sont absorbées par l'échantillon. Absorption: Certaines des longueurs d'onde incidentes sont (partiellement) absorbées dans l'échantillon, tandis que d'autres longueurs d'onde sont transmises sans beaucoup de perte d'intensité. (Schéma 3)
Fluorescence
La matière peut réémettre la lumière absorbée à nouveau par un processus indépendant appelé fluorescence. La lumière émise a une longueur d'onde différente et plus longue que la lumière initialement absorbée, ce qui entraînera une "amplification" perçue de certaines longueurs d'onde de la lumière. C'est un processus particulièrement courant pour les échantillons colorés et les grandes biomolécules. Fluorescence: La lumière verte incidente est absorbée (ce qui entraîne une perte d'intensité) et réémise dans des longueurs d'onde différentes et plus longues (ce qui entraîne un gain d'intensité ou même l'ajout de nouvelles « couleurs »). (Figure 4)
Diffusion
Lorsqu'une source de lumière intense (par exemple, un laser) frappe un échantillon, une partie de la lumière sera dispersée dans différentes directions. La majorité de la lumière diffusée a la même longueur d'onde (« couleur ») que la lumière incidente – elle est diffusée de manière élastique. C'est pourquoi l'œil humain est capable de "voir" le point d'un pointeur laser sur le mur ou la table. Cependant, une infime fraction de la lumière dispersée interagit avec la matière qu'elle touche d'une manière qui échange de petites quantités d'énergie, ce qui est appelé diffusion inélastique. Le changement d'énergie de la lumière diffusée entraîne une fréquence et une longueur d'onde modifiées. L'origine microscopique de cette interaction Raman est une excitation ou une désexcitation des vibrations moléculaires dans la matière. Les caractéristiques de ces vibrations déterminent la longueur d'onde de la lumière diffusée de manière inélastique. En mesurant la distribution d'intensité (spectre) de la lumière diffusée, il est donc possible de déduire des informations sur la structure vibratoire de la substance éclairée. La spectroscopie Raman appartient au groupe des spectroscopies vibratoires. Diffusion Raman: La plupart de la lumière jaune incidente est diffusée de manière élastique dans toutes les directions. De petites quantités de lumière, généralement avec des longueurs d'onde plus élevées (orange, rouge), sont également dispersées de manière inélastique après interaction avec les molécules de l'échantillon. (Figure 5)
Chacun de ces processus peut être exploité pour extraire des informations sur la nature chimique et physique de l'échantillon. Le type exact et l'étendue des propriétés moléculaires déductibles dépendent du type de spectroscopie utilisé. Les deux principales spectroscopies vibratoires sont la spectroscopie infrarouge (IR) et la spectroscopie Raman. La spectroscopie Raman utilise l'effet Raman pour l'analyse des substances. Les bases de la diffusion Raman sont expliquées ci-dessous.
Théorie de la diffusion Raman ("l'effet Raman")
Il existe trois processus de diffusion qui sont importants pour la spectroscopie Raman et les techniques d'imagerie Raman :[3]
Diffusion Raman anti-Stokes
Diffusion Raman anti-Stokes est un autre processus de diffusion inélastique. Ici, une quantité spécifique d'énergie est transférée d'une vibration moléculaire au photon. Le photon dispersé a une énergie plus élevée et une longueur d'onde plus courte que le photon incident. Ce processus est encore moins susceptible de se produire que la diffusion de Stokes. Par conséquent, il n'est généralement pas utilisé en spectroscopie Raman. Les informations extraites de la lumière diffusée anti-Stokes sont principalement équivalentes aux informations extraites de la lumière diffusée Stokes, et seules des applications très spécialisées nécessiteront l'effort supplémentaire de mesurer les deux processus de diffusion.
Diffusion Raman Stokes
Scoupures de diffusion Raman est le processus de diffusion inélastique qui transfère de l'énergie de la lumière à une vibration de la molécule. Cependant, le photon dispersé a une énergie plus élevée et une longueur d'onde plus courte que le photon incident. La quantité d'énergie transférée n'est pas arbitraire, elle doit être exactement la quantité requise pour exciter l'une des vibrations moléculaires de la molécule. La composition de la lumière diffusée dépend donc fortement du type exact de molécule (comme une empreinte digitale). La diffusion de Stokes est le processus le plus couramment exploité pour acquérir un spectre Raman. Il est, cependant, plusieurs ordres de grandeur moins probable qu'il se produise par rapport à la diffusion de Rayleigh, rendant sa détection difficile.
Diffusion de Rayleigh
Diffusion de Rayleigh est le terme utilisé pour la diffusion élastique de la lumière par des molécules, et c'est de loin le processus de diffusion le plus dominant. L'interaction ne change pas l'état énergétique de la molécule et, en tant que telle, le photon diffusé a la même couleur (longueur d'onde) que le photon incident. Dans un spectromètre Raman, la lumière diffusée de Rayleigh doit être éliminée de la lumière collectée, sinon elle obscurcirait les signaux Raman.
Spectroscopie vibratoire – interprétation d'un spectre Raman
Toutes les spectroscopies vibratoires caractérisent les vibrations moléculaires et, dans une moindre mesure, également les rotations moléculaires. Les vibrations moléculaires sont basées sur les mouvements des atomes individuels de la molécule les uns par rapport aux autres. Les forces maintenant la molécule ensemble agiront comme de petits ressorts reliant les atomes comme illustré dans la figure 6. L'ensemble des vibrations dépend fortement de la structure exacte de la molécule et comprend donc un spectre vibratoire unique. Cela fait de la spectroscopie vibratoire un outil idéal pour l'identification des substances. En fait, le spectre vibratoire est si unique qu'il (ou plus précisément une partie de celui-ci) est souvent appelé « l'empreinte chimique » de la molécule. Différentes spectroscopies vibratoires peuvent détecter un sous-ensemble différent du spectre vibratoire complet, c'est pourquoi les méthodes les plus courantes dans cette classe, Raman et (FT-)IR, sont souvent appelées "méthodes complémentaires".[1][2]
Quand une molécule est-elle active en Raman ?
La spectroscopie Raman détecte des changements dans la polarizabilité d'une molécule. Il ne détecte donc que les vibrations où la polarizabilité change pendant le mouvement (ce sont des vibrations actives en Raman)
- La polarizabilité décrit à quel point le nuage d'électrons autour d'une molécule peut être déformé.
- Un changement de polarizabilité est, par exemple, causé par une augmentation de la taille du nuage d'électrons.
- Un exemple d'un mouvement vibratoire augmentant la taille du nuage électronique (local) d'une molécule est une vibration de dilatation symétrique (figure 7).
Visualisation des spectres Raman
La pratique couramment acceptée est de tracer les spectres Raman dans un graphique "Taux de Comptage" vs. "Décalage Raman". Le décalage Raman est la différence d'énergie entre la lumière incidente (laser) et la lumière diffusée (détectée). Cette différence est alors uniquement liée aux propriétés énergétiques des vibrations moléculaires étudiées et donc indépendante de la longueur d'onde du laser. Le décalage Raman est généralement exprimé en nombres d'onde. Le taux de comptage est le nombre d'événements que le détecteur enregistre pour le décalage Raman respectif par seconde d'intégration du détecteur. Il est proportionnel à l'intensité de la lumière imagée au détecteur.
Interprétation des spectres Raman
Il existe plusieurs approches qui peuvent être utilisées pour interpréter les spectres Raman, y compris les trois décrites ci-dessous.
En identifiant des groupes fonctionnels au sein des molécules
Les vibrations de certaines sous-unités distinctes d'une molécule, appelées ses groupes fonctionnels, apparaîtront dans un spectre Raman à des décalages Raman caractéristiques. Un tel changement est similaire pour toutes les molécules contenant le même groupe fonctionnel. Ces signaux sont particulièrement utiles lors de la surveillance des réactions impliquant ces groupes fonctionnels (oxydation, polymérisation, etc.), car ils fournissent une mesure directe de l'avancement pendant la réaction. L'utilisation de ces décalages caractéristiques permet de relier le spectre d'un composé inconnu à une classe de substances, par exemple la vibration d'étirement du groupe carbonyle dans un aldéhyde se situe toujours dans la plage de 1730 cm–1 à 1700 cm–1. La figure 8 montre le spectre Raman du benzonitrile, contenant la vibration d'élongation du groupe cyano (CN) du benzonitrile à une valeur caractéristique de 2229,4 cm⁻¹..[4]
Utilisant la région caractéristique "empreinte digitale"
En dehors des vibrations moléculaires de groupes fonctionnels spécifiques, les vibrations de l'ossature moléculaire (vibrations squelettiques) peuvent être détectées dans un spectre Raman. Les vibrations squelettiques se trouvent généralement à des décalages Raman inférieurs à 1500 cm–1 et présentent un motif caractéristique spécifique à la substance. Cette région, souvent appelée la région « empreinte digitale » d'une substance, est la partie la plus importante du spectre à des fins d'identification.[5]
Avec un logiciel d'interprétation assistée par ordinateur
L'identification des substances par spectroscopie Raman est de nos jours effectuée à l'aide d'un logiciel contenant un algorithme de comparaison et une base de données spectrale. Le résultat est présenté comme un facteur de correspondance – l'Indice de Qualité de Frappe (HQI). Ce facteur varie de 0 (pour "aucun match") à 100 (pour "match exact"). L'utilisateur peut alors définir un seuil en dessous duquel le HQI est interprété comme une correspondance. De cette manière, l'identification des substances est possible en quelques secondes et les utilisateurs non techniques peuvent facilement interpréter les résultats.
Conclusion
La spectroscopie Raman est un type de spectroscopie vibratoire qui nécessite une bonne compréhension des propriétés de la lumière. Il fournit une "empreinte" chimique de la substance mesurée et est donc fréquemment utilisé chaque fois que des matériaux inconnus doivent être identifiés.
Cependant, obtenir un spectre Raman n'est que le début : après avoir visualisé les données, vous devez interpréter l'image Raman.
Pour plus d'informations sur le principe de mesure et les utilisations de la spectroscopie Raman, voir "Comment la spectroscopie Raman peut-elle vous aider ?"
Découvrez ici quel analyseur Raman serait le meilleur pour vous.
Références
1. Hollas, J. M. (2004). Spectroscopie moderne. 4ème Édition. Chichester, Royaume-Uni : John Wiley & Sons. 2. Long, D. A. (2002). L'effet Raman – Un traitement unifié de la théorie de la diffusion Raman par les molécules. Chichester, Royaume-Uni : John Wiley & Sons. 3. McCreery, R. L. (2000). Spectroscopie Raman pour l'analyse chimique. New York, France : John Wiley & Sons. 4. ASTM E1840-96 (2014) 5. Hesse, M., Meier, H. et Zeeh, B. (2005). Méthodes spectroscopiques en chimie organique. Stuttgart : Georg Thieme Verlag.











