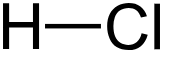Le tableau 1 contient une liste partielle des acides courants, ainsi que leurs formules chimiques et applications.
Tableau 1 : Acides courants et leurs applications
| Nom chimique | Formule chimique | Applications |
| Acide chlorhydrique | HCl | Affinage des métaux, décapage de l'acier, production de chlorures métalliques, contrôle du pH de l'eau de process et neutralisation des flux de déchets, nettoyage ménager, régénération des échangeurs d'ions (ChemicalSafetyFacts, 2022) |
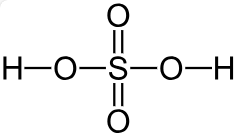
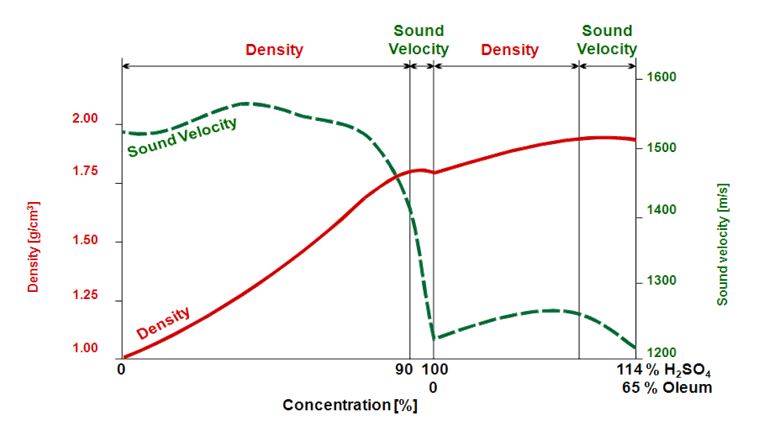
| Acide sulfurique | H2SO4 | Dans les batteries de voiture, la fabrication d'engrais, la production de détergents, de résines synthétiques, de colorants, de produits pharmaceutiques, de catalyseurs pétroliers et d'insecticides (Les Éditeurs de l'Encyclopædia Britannica, 2024) |
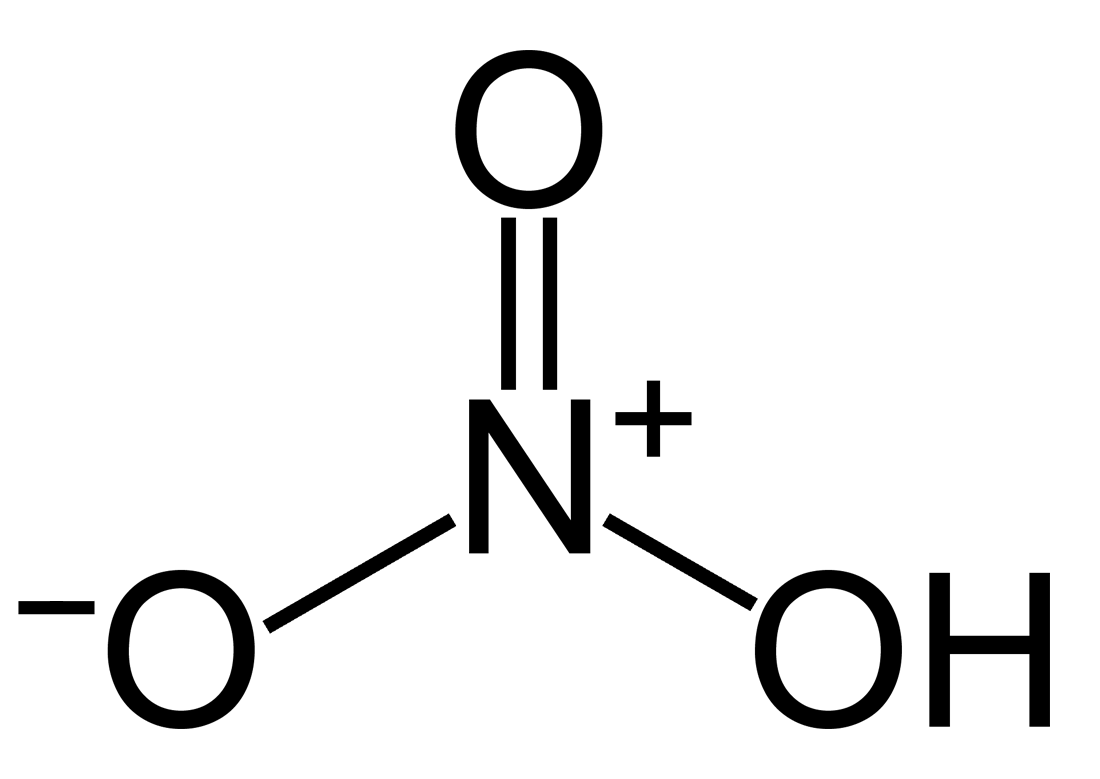
| Acide nitrique | HNO3 | Fabrication d'engrais, d'explosifs, de précurseurs de nylon et de composés organiques, en tant que propergol de fusée, lors du traitement des métaux, séparation de l'or (PubChem, pas de date) |
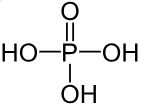
| Acide phosphorique | H3PO4 | Fabrication d'engrais, acidification des aliments et des boissons, en tant que conservateur, pour le polissage chimique de l'aluminium et la passivation de l'acier, en tant qu'agent désinfectant dans les industries laitières, alimentaires et de la brasserie (PubChem, pas de date) |
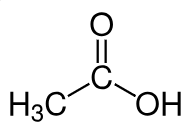
| Acide acétique | CH3COOH | Réactif chimique pour la production d'acétate de vinyle, d'esters et d'anhydride acétique, en tant que solvant et vinaigre (Brown, 2024) |
| Acide fluorhydrique | HF | Production de composés organofluorés et de fluorures inorganiques, en tant qu'agent de gravure dans l'industrie des semi-conducteurs (CDC, 2018) |