Matériaux nanobiologiques

Lorsqu'on parle de nanomatériaux biologiques, on pense généralement aux nanoparticules. Lorsqu'on parle de nanomatériaux biologiques, on pense généralement aux nanoparticules, mais d'autres types de nanomatériaux se sont également révélés très utiles pour des applications telles que l'administration de médicaments, la médecine régénérative et bien d'autres encore. Dans cette section, vous trouverez un cas de recherche qui décrit la caractérisation structurelle des macromolécules biologiques en solution avec SEC-SAXS. De plus, vous trouverez des articles sur la diffusion de la lumière dynamique et électrophorétique des virus et des particules semblables aux virus ainsi que des exosomes, ainsi que des tests de viscosité des biomatériaux pour la nanomédecine. Toutes ces techniques sont très précieuses pour la recherche sur les nanomatériaux biologiques. Anton Paar offre non seulement les instruments pour les techniques, mais aussi un soutien et une expertise précieux – pour faire avancer votre recherche.
SEC-SAXS – Caractérisation structurale des macromolécules biologiques en solution
Introduction
Les interactions moléculaires sont importantes pour le fonctionnement des assemblages et systèmes macromoléculaires biologiques. La diffusion des rayons X à petit angle (SAXS) peut fournir des informations structurelles et dynamiques clés pour les macromolécules biologiques telles que les protéines, et les acides nucléiques et leurs complexes en solution, dans des conditions quasi-natives. Une condition préalable à l'interprétation précise des données SAXS de la solution est que la macromolécule étudiée soit présente sous forme monodisperse. Ce n'est qu'alors qu'il est possible de dériver la structure tridimensionnelle des protéines en haute qualité. En pratique, de nombreux échantillons comprennent des structures agrégées et des mélanges oligomériques, respectivement, ce qui complique une évaluation précise des données de diffusion. Pour surmonter ce problème, la SAXS peut être couplée à la chromatographie par exclusion de taille (SEC) et fournit ainsi un outil efficace pour le dépistage et les études structurelles d'échantillons biomoléculaires. SEC – qui est souvent la dernière étape de nombreux protocoles de purification des protéines – sépare les biomolécules en fonction de leurs propriétés hydrodynamiques (taille, forme). La méthode est suffisamment spécifique pour séparer même différentes espèces oligomériques, telles que les monomères, les dimères et les oligomères supérieurs.Montage expérimental
Les capacités de la SEC-SAXS combinée ont été démontrées en séparant et en analysant des solutions protéiques mixtes complexes d'albumine sérique humaine (HSA) et de lysozyme par couplage en ligne ainsi qu'hors ligne. Un système Äkta Pure 25 FPLC a été utilisé pour séparer les mélanges de protéines, tandis que les données SAXS des fractions de protéines élues ont été mesurées avec un système Anton Paar SAXSpace. Pour le traitement automatique des données SEC-SAXS mesurées, une analyse en composantes principales (ACP) et une analyse discriminante par moindres carrés partiels (PLS-DA) ont été utilisées. PCA et PLS-DA sont des techniques statistiques multivariées permettant l'analyse automatique d'échantillons de protéines complexes posant plusieurs défis, par ex. des concentrations variables, des espèces biomoléculaires variables au cours de la course SEC, et une co-élution potentielle de différentes biomolécules.Résultats et discussion
Des mélanges de protéines complexes ont été séparés et mesurés avec succès à l'aide de SEC-SAXS avec des instruments de laboratoire, ce qui a permis une séparation efficace des différentes fractions de protéines. Les données de diffusion mesurées ont été évaluées à l'aide d'une ACP et d'une PLS-DA. Notamment, les pics de fractions étroitement éludées et de différentes biomolécules pouvaient être automatiquement discriminés, sans nécessiter d'analyse manuelle des données. Par conséquent, même des échantillons de protéines complexes comprenant de grands agrégats ainsi que des mélanges de différents oligomères pourraient être analysés efficacement.

Informations complémentaires
Instruments :- SAXSpace
- SAXSpoint 5.0
Rapports d'application :
- Couplage de la chromatographie par exclusion de taille et de la diffusion des rayons X à petit angle – Principes et applications
- SEC-SAXS en ligne de la protéine HSA à l'aide d'un instrument SAXS de laboratoire
Investigation du virus inactivé et des particules semblables au virus
Introduction
La plupart des vaccins antiviraux sont constitués de virus inactivés, de protéines recombinantes ou de particules semblables à des virus qui n'ont aucun potentiel de réplication. C'est pourquoi nombre d'entre eux sont administrés avec des adjuvants vaccinaux, qui augmentent l'efficacité et la longévité de la réponse immunitaire. L'adjuvant le plus ancien et encore le plus utilisé est le sel d'aluminium (par exemple, hydroxyde d'aluminium). L'immunogénicité du vaccin est fortement liée à la taille des particules. À quelques exceptions près, les virus sont des nanoparticules dont la taille varie de 15 à 300 nm. Lors de l'injection, les particules de cette taille sont efficacement absorbées par les cellules dendritiques, une catégorie de cellules sentinelles dotées de la capacité unique d'induire une immunité médiée par les anticorps et les cellules tueuses. En revanche, les particules de l'ordre du micromètre, telles que les particules de sel d'aluminium, sont préférentiellement absorbées par les monocytes et les macrophages, qui induisent principalement une réponse immunitaire médiée par les anticorps. Par conséquent, la taille des particules du vaccin doit être surveillée et adaptée en fonction du type de réponse immunitaire requise pour contrer le pathogène. Le potentiel zêta donne des informations supplémentaires pour le contrôle de la qualité des préparations de vaccins.Montage expérimental
Échantillons : vaccin inactivé contre l'encéphalite à tiques (TBE), basé sur la souche de Neudörfl et adjuvanté avec de l'hydroxyde d'aluminium. Vaccin grippal quadrivalent contenant 2 souches de virus grippaux A et 2 souches de virus grippaux B, conformément aux directives de l'OMS pour la saison grippale 2019-2020 de l'hémisphère nord. Échantillon de traitement : Les vaccins ont été mesurés après un stockage continu à +4 °C ainsi qu'après un conditionnement à 50 °C (« traité à la chaleur ») ou à -18 °C (« décongelé ») pendant 24 h. Technique de caractérisation : Les nanoparticules de protamine miARN finales ont été caractérisées par la taille des particules et le potentiel zêta avec le Litesizer 500.Résultats et discussion
Le vaccin TBE stocké à 4 °C présente un pic unique culminant entre 2 µm et 3 µm correspondant à la taille des particules d'hydroxyde d'aluminium commercial utilisé comme adjuvant de vaccin. Il est intéressant de noter qu'une augmentation significative de l'HDD est observée à la fois pour les échantillons de vaccins traités à la chaleur et pour les échantillons congelés-décongelés, ce qui indique que les perturbations majeures de la chaîne du froid favorisent l'agrégation des adjuvants. Cela suggère que la congélation-décongélation tend à augmenter l'agrégation des particules virales divisées, tandis que le traitement thermique la réduit. Les deux vaccins montrent un potentiel zêta légèrement négatif (faible magnitude) qui, d'une part, pourrait favoriser l'absorption par les cellules sentinelles, mais pourrait également expliquer leur tendance à s'agréger en réponse aux perturbations de la chaîne du froid.Paramètres | Non traité | Traitement thermique | Congelé-décongelé |
Moyenne ZP | - 6,6 mV | - 6,0 mV | - 5,7 mV |
Déviation standard | 0.9 mV | 0.8 mV | 1.3 mV |
Déviation standard [%] | 13.7 % | 12.5 | 22.4 % |


Informations complémentaires
Instruments :Rapport d’application
- Giving It Its Best Shot : Contrôle qualité des vaccins antiviraux avec le Litesizerhttps://www.anton-paar.com/?eID=documentsDownload&document=69713
Exosomes comme nouvelles frontières dans la délivrance de médicaments
Introduction
Les exosomes sont des vésicules de taille nanométrique qui peuvent être isolées du milieu de culture cellulaire ainsi que de nombreux fluides extracellulaires tels que le sang, l'urine, la salive, le lait maternel et le liquide céphalorachidien. Leur potentiel en tant que système de délivrance de médicaments est connu depuis des années. Leurs nombreux avantages incluent une action de ciblage cellulaire à longue portée, une faible toxicité, une faible immunogénicité, une grande stabilité et la capacité d'encapsuler des protéines, des médicaments ou des acides nucléiques. Pour cette raison, les exosomes sont considérés comme de nouvelles frontières dans le développement de vaccins et de thérapies ciblant le cancer. Comme indiqué dans ce rapport, la caractérisation des exosomes par la taille des particules ainsi que le potentiel zêta permet de surveiller la stabilité, d'optimiser les conditions de stockage et d'estimer le processus d'absorption des cellules cibles.Montage expérimental
Préparation de l'échantillon : Le milieu de culture cellulaire utilisé pour la lignée cellulaire humaine TR146, un carcinome épidermoïde provenant de la muqueuse buccale (de Cancer Research UK), a été aspiré et centrifugé. Les exosomes ont été isolés avec le kit d'isolement total des exosomes Invitrogen™ (Thermo Fisher Scientific). Les échantillons ont été incubés au réfrigérateur toute la nuit puis centrifugés à 10 000 g pendant 60 min à 4 °C. Le surnageant résultant a été éliminé et le culot d'exosomes a été resuspendu dans 100 µL de tampon PBS (pH = 7,4, Thermo Fisher Scientific). Technique de caractérisation : Les nanoparticules de protamine miARN finales ont été caractérisées par la taille des particules et le potentiel zêta avec le Litesizer 500.Résultats et discussion
Les résultats de la distribution de la taille des particules de la suspension d'exosomes non traitée ont affiché 3 pics bien définis, avec un pic de grandes particules (~ 200 nm) correspondant aux débris cellulaires, un pic de particules de taille moyenne (~ 30 nm) correspondant aux exosomes, et un pic discret de très petites particules (~ 2 -10 nm) indiquant la présence de protéines en suspension. La taille moyenne des particules du pic d'exosomes n'a enregistré que de légères fluctuations au cours d'une semaine de stockage à 4 °C. Pour les échantillons stockés à 37 °C, la taille des particules des exosomes avait déjà diminué de manière significative après 72 heures. Les résultats du potentiel zêta fournissent des informations sur la charge de surface des exosomes et donc sur leur interaction avec les systèmes biologiques.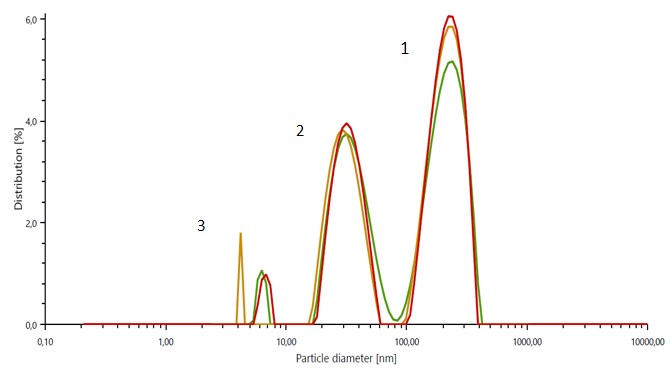

Informations complémentaires
Instruments :Rapport d’application
Test de viscosité des biomatériaux comme l'argile de bentonite pour la nanomédecine
Introduction
La fonctionnalisation de surface des matériaux pour une interaction contrôlée avec divers systèmes d'intérêt biologique est d'une importance vitale ; les biomatériaux subissent une nano- et microstructuration pour leur utilisation finale en nanomédecine.Montage expérimental
500 mL d'argile bentonite ont été versés dans un bécher de 600 mL et testés en viscosité à l'aide d'un viscosimètre rotatif. Un adaptateur de support motorisé pour le viscosimètre rotatif et les broches en T a été utilisé pour la mesure en raison du comportement pâteux du matériau au repos. Une rampe de vitesse linéaire de 1 tr/min à 10 tr/min avec 4 points de mesure a été réalisée pour évaluer le comportement d'écoulement. La durée du point de mesure a été fixée à 1 min et 30 sec. L'adaptateur de support motorisé a créé un mouvement hélicoïdal de l'arbre en T dans l'échantillon et a éliminé le problème de « canalisations ». Tout autre axe qui tourne à la même hauteur créerait un canal d'air à l'intérieur d'un tel échantillon. Cela conduirait à des valeurs de viscosité sans signification, car seule une partie de l'échantillon est en contact avec le mandrin.Résultats et discussion
Comme prévu, l'argile bentonite a présenté un comportement d'écoulement en cisaillement réducteur avec un indice de cisaillement réducteur de 8,3519. Cela signifie que la viscosité de l'échantillon est devenue plus faible à des taux de cisaillement plus élevés. Avoir le comportement d'écoulement à cisaillement réducteur approprié (et ajuster les ingrédients en conséquence) simule, par exemple, un humain déglutissant un produit de nanomédecine. Le comportement final de l'écoulement peut être ajusté en augmentant la concentration de poudre de nanoparticules ou en ajoutant de l'argile bentonite comme agent épaississant, si nécessaire.Informations complémentaires
Instruments :Rapport d’application