Matériaux 2D

Les matériaux monocouches sont au centre des recherches pour des applications très polyvalentes. Cela inclut des jauges de contrainte de taille nanométrique, des revêtements nanocristallins de TiO2 pour les implants corporels, ou, par exemple, l'étude de la cristallinité de matériaux 2D de l'anode ou de composants cathodiques afin de favoriser un transfert d’énergie plus rapide et plus efficace dans les batteries. Dans cette section, nous montrons comment diverses solutions de mesure et différentes technologies d'Anton Paar jouent un rôle important dans la caractérisation des matériaux 2D telles que la diffusion des rayons X aux petits angles en incidence rasante à température contrôlée (GISAXS) pour étudier les propriétés thermiques des structures de films minces auto-assemblés, le potentiel zêta de surface pour étudier l'adsorption de protéines sur les revêtements d'anatase TiO2 , ou encore l'utilisation de la pycnométrie à gaz pour mesurer la densité squelettique d'une série de graphènes présentant des degrés de cristallinité variables.
Caractérisation des nanostructures 2D de nanoparticules d'or auto-assemblées
Introduction
Les nanoparticules colloïdales sont largement utilisées en raison de leurs propriétés électroniques, chimiques et biologiques spécifiques. Par exemple, l'or colloïdal (Au) peut former des structures bidimensionnelles et tridimensionnelles comprenant des monocouches de nanoparticules d'or arrangées selon un réseau hexagonal. De tels matériaux constituent des systèmes prometteurs pour, par exemple, des jauges de contrainte de taille nanométrique. L'applicabilité de tels matériaux en couche mince peut bien sûr être limitée par la stabilité mécanique ou thermique. Ainsi, une méthode in situ telle que la diffusion des rayons X aux petits angles en incidence rasante à température contrôlée (GISAXS) est un outil idéal pour étudier les propriétés thermiques de ces structures de couches minces autoassemblées.Montage expérimental
Une couche homogène de nanoparticules d'Au disposées de manière hexagonale a été déposée sur des substrats en plaquettes de Si en utilisant une méthode Langmuir-Schaefer . Les films minces obtenus ont été mesurés avec un système Anton Paar SAXSpoint équipé d'une scène GISAXS dédiée et d'un module de chauffage. Les changements structurels de l'échantillon ont été surveillés de la température ambiante jusqu'à 220 °C. Pour une évaluation précise des motifs de diffusion GISAXS, BornAgain [1] est actuellement le logiciel le plus avancé – il permet la simulation des données GISAXS. Avec une routine d'exportation de données dédiée, les données GISAXS acquises avec le système SAXSpoint peuvent être directement transférées vers la plateforme BornAgain.Résultats et discussion
À température ambiante, le motif GISAXS acquis a montré que le monolayer d'Au auto-assemblé avait un agencement typique compact hexagonal (hcp). Dans in-situ les expériences de chauffage GISAXS, cette structure s'est avérée stable à des températures allant jusqu'à 180 °C, prouvant la bonne stabilité de ce système. Au-dessus de 180 °C, une transformation des petites nanoparticules d'Au en tailles plus grandes a été observée, entraînant une nanostructure stable au-dessus de 195 °C. Cela prouve que in-situ GISAXS est un outil précieux pour surveiller la structure, la stabilité et les changements structurels de telles structures 3D de taille nanométrique. Pour une évaluation détaillée, les motifs GISAXS de l'échantillon présentant hcp arrangements ont été automatiquement exportés et analysés avec le logiciel BornAgain. L'ajustement calculé par rapport aux données expérimentales a révélé une taille de particule d'environ 6 nm pour les nanoparticules d'Au, et une constante de réseau d'environ 8 nm [2].

Informations complémentaires
Instruments :- SAXSpoint
Références
- www.bornagainproject.org
- K. Vesgo, M. Jergel, P. Siffalovic, M. Kotlar, Y. Halahovets, M. Hodas, M. Pelletta, E. Majkova, Capteurs et Actionneurs A : Physique 241 (2016) 87-95.
Rapports d'application :
Adsorption de protéines sur des revêtements de TiO₂ nanocristallin
Introduction
Les matériaux à base de Ti sont parmi les matériaux les plus couramment utilisés pour le remplacement des tissus durs, car ils offrent des propriétés mécaniques et chimiques appropriées. Cette étude se concentre sur l'adsorption des protéines sur les revêtements d'anatase TiO2 et l'influence de l'irradiation UV avant l'adsorption des protéines. Les résultats rapportés donnent des informations détaillées sur la caractérisation du potentiel zêta de surface des revêtements nanocristallins de TiO2 pour les implants corporels, et fournissent ainsi une base pour des études liées à l'hémocompatibilité et à la biocompatibilité de cette classe de matériaux.Montage expérimental
Des disques de TiO2 commercialement pur (cp) et traités par hydrothermie (HT) ont été utilisés comme matériau de base pour la conduction de mesures de potentiel zêta et d'études cinétiques d'adsorption avec un SurPASS. PBS a servi de solution électrolytique. Les courbes de titration de pH ont été obtenues en utilisant HCl comme acide et NaOH comme base. L'albumine sérique bovine (BSA) a été utilisée comme protéine pour l'étude de l'adsorption résolue dans le temps.Résultats et discussion
Tous les échantillons avaient un point isoélectrique (PIE, valeur de pH où le potentiel zêta est de 0 mV et un renversement de charge se produit) à un pH acide, et un potentiel zêta négatif à un pH physiologique, avec le potentiel zêta négatif le plus élevé se produisant pour l'échantillon cp. Cette observation peut être liée à la structure d'oxyde amorphe des échantillons HT, qui a modifié la densité et la stabilité des groupes hydroxyles de surface. L'exposition au BSA a entraîné un déplacement du IEP à une valeur de pH d'environ 5, confirmant la couverture complète de toute la surface de TiO2 investiguée avec la protéine globulaire. Bien que la forme des courbes de titration n'ait pas permis d'autres conclusions sur le comportement d'adsorption, la cinétique d'adsorption recodée a fourni des aperçus plus profonds et a révélé le taux d'adsorption le plus rapide pour l'échantillon HT pré-irradie UV, avec des taux progressivement plus bas jusqu'à l'échantillon cp.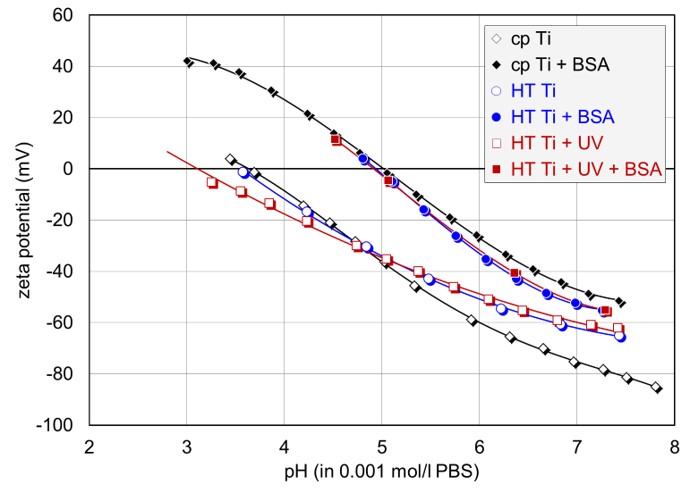

Informations complémentaires
Instruments :Source: S. Novak et al., Biomed. Mater. 10 (2015) 045012
Caractérisation de surface des monolayers auto-assemblés déposés sur des substrats en or
Introduction
Les monocouches autoassemblés (SAMs) sont des assemblages formés spontanément de molécules organiques adsorbées sur des surfaces solides, et permettent de contrôler leurs propriétés physico-chimiques. Ce type de nanomatériau est un candidat intéressant pour ajuster les propriétés de surface des interfaces biologiques et biotechnologiques, comme les biosenseurs, car il n'affecte ni l'épaisseur de l'échantillon ni les propriétés électriques volumétriques des matériaux. Cette étude se concentre sur l'investigation des SAMs organiques avec différentes fonctionnalités et sur la caractérisation du potentiel zêta de surface. Cette relation peut fournir des informations précieuses sur l'interaction électrostatique des SAMs avec des matériaux de taille nanométrique, et peut déclencher leur adsorption et désorption.Montage expérimental
Échantillons investigués:SAMs à base de thiol avec COOH pur, NH2pur, et fonctionnalité mixte déposés sur des substrats en or. Technique de caractérisation :
les mesures du potentiel zêta de surface ont été réalisées avec l'analyseur électrocinétique SurPASS équipé d'électrodes Ag/AgCl et de la cellule à écartement réglable pour des échantillons plans. Une solution d'électrolyte 0,1 mM NaCl a été utilisée. Les courbes de titration de pH ont été obtenues en ajoutant un acide (HCl) et une base (NaOH) à la solution électrolytique.
Résultats et discussion
Les SAMs à base de thiol avec différents rapports de groupes terminaux amine et carboxyle ont été caractérisés en fonction de leur potentiel zêta de surface. L'étude du potentiel zêta par rapport à la valeur du pH a révélé un changement clair dans le point isoélectrique (PIE, valeur du pH où le potentiel zêta est de 0 mV et un renversement de charge se produit) avec un rapport changeant de groupes fonctionnels. Plus le contenu en amines est élevé, plus le pH IEP a été déplacé de l'acide vers le pH neutre. Cependant, l'augmentation de l'IEP n'était pas linéaire avec le rapport des groupes terminaux ; néanmoins, la contribution de la fonctionnalité COOH dominait. Cela peut être lié au fait que la chaîne carbonée de COOH est plus longue et donc plus facilement accessible par rapport à la chaîne de NH2 comme le montre la Figure 2.

Informations complémentaires
Instruments :Source: *Shyue et al., Phys. Chem. Chem. Phys. 11 (2009) 6199-6204
Cristallinité du graphène et relation avec les propriétés de transfert d'électrons de la batterie
Introduction
L'amélioration des composants des batteries à électrodes pour obtenir un transfert d'énergie plus rapide et plus efficace est une partie importante de la recherche et de la conception des matériaux de batterie. En particulier, la cristallinité est une propriété critique des composants d'électrodes de batteries solides car elle permet aux ions de conduire efficacement à travers l'anode et la cathode au lieu de se ralentir dans les domaines amorphes. Plus la cristallinité du composant anodique ou cathodique est élevée, plus le transfert d'électrons à travers et entre les composants est efficace. Ici, nous utilisons la pycnométrie à gaz pour mesurer la densité squelettique d’une série de graphènes présentant des degrés de cristallinité variables, où une densité squelettique plus élevée correspond à un matériau plus cristallin.Montage expérimental
Techniques de caractérisation : Des mesures de densité squelettique d'une série de graphènes ont été effectuées à l'aide d'un pycnomètre à gaz Anton Paar Ultrapyc 5000. En raison de la nature poreuse de ces carbones, les échantillons ont été dégazés sous vide pendant 3 heures à température ambiante sur un dégazeur externe avant d'être transférés dans la cellule d'échantillonnage de l'instrument. Les échantillons ont ensuite été conditionnés à l'intérieur du pycnomètre en utilisant un flux de gaz purgé à l'hélium pendant 3 min. Les expansions de gaz ont été effectuées en utilisant de l'hélium à partir d'une pression de départ de 1,17 bar.Résultats et discussion
Les densités squelettiques de 3 carbones d'électrode différents ont été trouvées à 2,117 g/cm3, 2,139 g/cm3, et 2,152 g/cm3. Les données du tableau ci-bas montrent que la densité peut être mesurée avec une excellente répétabilité, < 1% pour tous les échantillons. En comparant les trois échantillons, la densité augmente de l'échantillon A à l'échantillon B puis à l'échantillon C. Il est connu que l'augmentation de la cristallinité est corrélée à une augmentation de la densité squelettique, ainsi l'échantillon 3 est le plus cristallin de ces trois échantillons de carbone d'électrode. Plus la cristallinité est élevée, plus le matériau est efficace pour le transfert d'électrons, ce qui fait de l'échantillon C le meilleur choix pour une anode de batterie.Échantillon | Masse volumique (g/cm3) | Répétabilité (%) | |||
| Course 1 | Course 2 | Course 3 | Moyenne |
|
A | 2,120 | 2,114 | 2,118 | 2,117 | 0.11 |
B | 2,138 | 2,139 | 2,139 | 2,139 | 0,02 |
C | 2,144 | 2,158 | 2,154 | 2,152 | 0,27 |
Informations complémentaires
Instruments :Rapport d’application