マイクロ波合成

「マイクロ波は21世紀のブンゼンバーナーになる可能性を秘めている」C. Oliver Kappe(オーストリア、グラーツ大学)
熱は化学反応を促進するため、化学合成において非常に重要です。ただし、熱を加えないと合成がうまくいかないこともあり、うまくいったとしても、室温では数日、数週間かかるのに対し、高温では数時間、数十分で終わることもあります。化学合成では、熱を加える代表的な手法として、ホットプレートを用いた従来の還流加熱とマイクロ波加熱があります。
従来の還流合成に比べ、最新のマイクロ波リアクターによるマイクロ波合成は、収率を高めながら、反応時間をわずか数分まで大幅に短縮することができます。さらに、最新のマイクロ波リアクターの安全性と利便性も、より多くの化学者が日々の研究業務でマイクロ波加熱を使用する理由となっています。
マイクロ波合成:関連情報

時間のかかる還流式から、便利で効率的な密閉容器での反応処理に切り替えたいとお考えですか?このコンバーターは、何から始めればいいのかヒントを提供してくれます。

個々の要件に最適なマイクロ波または従来型の加熱密閉容器式リアクターを検索できます。
マイクロ波合成に関する詳細はこちら
マイクロ波化学の歴史
ロベルト・ブンゼンが、1855年にかの有名なバーナーを発明すると、この熱源からのエネルギーを集中的に反応容器に応用できるようになりました。このブンゼンバーナーは、後にオイルバスやホットプレートに置き換わります。21世紀では、マイクロ波エネルギーによる反応が、科学界でますます注目されています。[1-4]
マイクロ波エネルギーは、もともと食品の加熱に使われていました。パーシー・スペンサーが1940年代に初めて使用しましたが、マイクロ波加熱を使用した化学合成の促進に関する最初のレポートが発表されたのは、1980年代半ばになってからでした。[5-6] 当初、実験は通常、家庭用の電子レンジでテフロンやガラスの密閉容器を用いて、温度や圧力を測定せずに行われていました。しかし、密閉された容器内で有機溶媒が急速に加熱されるため、しばしば激しい爆発を起こすことがありました。それでも、マイクロ波合成の最初の15年間は、家庭用の電子レンジが化学合成に多用されていました。

図1は、2種類のグラフを示しています。1つ目のグラフ(灰色の棒グラフ)は、マイクロ波化学が誕生してから20年の間に、「マイクロ波」をキーワードにした論文の数が大幅に増加したことを表しています。2つ目のグラフ(黒色の棒グラフ)は、専用リアクター(=科学用に開発されたリアクター)を化学合成に使用した論文を全文検索した結果です。[8]
論文数が指数関数的に増加していることから明らかなように、専用リアクターが市場に導入されてから、マイクロ波化学への関心が飛躍的に高まっています。これには明白な理由がありました。つまり、家庭用電子レンジでは安全性に欠け、反応パラメーターの測定も十分に正確ではなかったことから、ほとんどの権威ある学術誌(米国化学会誌など)は、台所用電子レンジの使用が記載されている原稿を審議しなくなったのです。[8]
結果として、専用のマイクロ波リアクターのユーザー数は現在も増え続けています。同時に、ほとんどの化学研究室には、適切なマイクロ波合成装置が備わっています。[7] このことを明確に示すのは、2008年以降、キーワードとして「マイクロ波」に言及した論文が大幅に減少しながらも(図1、灰色の棒グラフ)、全文検索の結果では、毎年1,000~1,200件増加しているという事実です。[9]
したがって、マイクロ波加熱はもはや特筆すべき珍しいものではなく、ホットプレートやロータリーエバポレーターなどの通常の実験器具と同様に、反応混合物の加熱に完全に定着した標準手法となっています。[7]
還流加熱からマイクロ波加熱へ
化学研究室での古典的な加熱は、熱源としてホットオイルバスを用いて反応混合物を還流させて行われることが多く、反応温度は通常、使用する溶媒の沸点に左右されます。まず、熱エネルギーがホットオイルバスから反応容器の表面に移動し、次に、高温の表面が反応容器の内容物を加熱します(図2の項目aを参照)。加圧できない開放系であるため、沸点を超える温度に加熱することは不可能です。

高温になった表面は局所的な過熱を招き、感度の高い物質を分解する可能性があります。さらに重要なことは、従来の化学反応には時間がかかることが多く、エネルギー効率が悪いということです(化学合成に数時間かかることは珍しくありません)。反応が終わり、すべての出発物質が変換されるのに、一晩あるいは週末が費やされることもあります。
このプロセスを加速させる鍵は、アレニウスの法則にあります。温度を10°C上げると、反応速度は2倍になり、反応がずっと早く終わるのです(例えば、わずか20°Cの温度上昇でも、反応時間が4分の1に短縮されます)。
例:
沸騰エタノール(約80°C)で8時間かかる反応も、160°Cの場合は約2分で終わらせることができます(表1参照)。
| 反応温度 | 80 ℃ | 90 ℃ | 100 ℃ | 110 ℃ | 120 ℃ | 130 ℃ | 140 ℃ | 150 ℃ | 160 ℃ |
|---|---|---|---|---|---|---|---|---|---|
| 反応時間 | 8 h | 4 h | 2 h | 1 h | 30 min | 15 min | 8 min | 4 min | 2 min |
表1:アレニウスの法則による時間短縮の目安。反応温度が10°C上昇すると反応時間は半分になります。
この原理は、市販のマイクロ波合成装置やマイクロ波サンプル前処理装置のすべてに採用されています。
反応容器は蓋をして封止し、反応混合物の沸点を超える温度まで加熱します。マイクロ波照射は、反応混合物中に存在する双極子やイオンとマイクロ波エネルギーが直接結合することで、エネルギー効率の高い内部加熱を実現します。マイクロ波は、(ほぼ完全に)マイクロ波透過性の容器の壁を通過し、分子(溶媒、試薬、触媒など)との直接的な相互作用により、反応混合物を分子単位で加熱します。このように直接「インコア」加熱(容器表面を最初に加熱しない)を行うため、マイクロ波照射は従来の加熱システムと逆の温度勾配になります(図2の項目bを参照)。
マイクロ波照射では非常に高い温度にできるため、従来は数時間、数日かかっていた反応時間を短縮し、数分で反応生成物を生成することができます。 また、目的温度まで急速に加熱するため、副生成物の形成も抑制されます。
マイクロ波加熱の原理
電磁スペクトル

マイクロ波照射とは,0.3~300 GHzの周波数範囲で,1 mm~1 mの波長に相当する電磁波を照射することです(図2を参照). 家庭用電子レンジや市販の化学合成専用マイクロ波リアクターは,すべて2.45 GHzの周波数(12.25 cmの波長に相当)で作動しています.
正確に計算すると,マイクロ波の照射エネルギーは分子結合を切断するには低すぎます.[7] したがって,マイクロ波のパワーを直接吸収して化学反応を「誘発」することは明らかに不可能なのです. しかし,マイクロ波照射は,化学合成に非常に有利な独自の熱効果をもたらします.分子結合を切断して化学反応を誘発することは,より高いエネルギーの照射(紫外線や可視光など→光化学)でなければできません.
マイクロ波誘電加熱
マイクロ波化学は,誘電加熱効果による物質(ほとんどの場合は溶媒)の効率的な加熱をベースとしています. 誘電加熱は,2つの主要なメカニズムで機能しています.
- 双極子分極(図3を参照) マイクロ波を照射したときに物質が発熱するには,その物質が双極子であること,つまり分子構造の一部がマイナスに,一部がプラスに帯電している必要があります. マイクロ波の電界は振動しているため,電界中の双極子は振動している電界に合わせて整列します. この整列によって回転が起こり,摩擦が生じ,最終的には熱エネルギーとなります.
- イオン伝導(図3を参照) イオン伝導では,(完全に)溶解した荷電粒子(通常はイオン)がマイクロ波照射の影響を受けて前後に振動します. この振動により,荷電粒子が隣接する分子や原子と衝突し,最終的に熱エネルギーが発生します.例えば,同量の蒸留水と水道水をマイクロ波で加熱した場合,水道水の方が水分子の双極子回転に加えてイオンを含んでいるため,より急速な加熱が起こります.

気体や固体のマイクロ波加熱は…
…ほぼ不可能です. 気体は,回転する分子間の距離が広すぎるため,マイクロ波を照射しても加熱できません. 同様に,氷のような固体物質は,水の双極子が結晶格子内で結合していて,液体状態のように自由に動けないため,マイクロ波が(ほぼ)透過してしまいます. ただし,炭化ケイ素のように,電子が自由に動ける導電性の固体物質は,マイクロ波の吸収に優れているため,非常に早く発熱します.
誘電特性

「誘電加熱」という言葉が示すように,マイクロ波で効率的に加熱するには,ある物質が特定の誘電特性を持っている必要があります. マイクロ波照射条件下での特定の物質(例えば溶媒)の加熱特性は,特定の物質が電磁エネルギーを熱に変換する能力に依存しています. この能力は,いわゆる損失正接,tanδによって決定します(図4).
一般的に使用されている有機溶媒のtan δ値を表2にまとめています.この表は,溶媒のマイクロ波吸収性を高(tan δ > 0.5),中(tan δ 0.1~0.5),低(tan δ < 0.1)に分類したものです. ベンゼンやジオキサンのような双極子モーメントを持たない溶媒は,多かれ少なかれマイクロ波透過性を持っています(tan δ < 0.01).
マイクロ波で急速に加熱するには,高いtan δ(表1を参照)を持つ溶媒が必要です. しかし,tan δ値の低い溶媒がマイクロ波合成に使用できないというわけではありません. 基質または試薬/触媒のいずれかに極性がある可能性が高いので,溶媒が無極性であっても,反応混合物の全体的な誘電特性によって多くの場合はマイクロ波による十分な加熱が可能です. しかし,混合物が無極性の場合は,加熱プロセスを助けるためにパッシブな発熱体を加えることができます.
| 高(> 0.5) | 中(0.1~0.5) | 低(< 0.1) | |||
| 溶媒 | tan δ | 溶媒 | tan δ | 溶媒 | tan δ |
| エチレングリコール | 1.350 | 2-ブタノール | 0.447 | クロロホルム | 0.091 |
| エタノール | 0.941 | ジクロロベンゼン | 0.280 | アセトニトリル | 0.062 |
| DMSO | 0.825 | NMP | 0.275 | 酢酸エチル | 0.059 |
| 2-プロパノール | 0.799 | 酢酸 | 0.174 | アセトン | 0.054 |
| ギ酸 | 0.722 | DMF | 0.161 | THF | 0.047 |
| メタノール | 0.659 | ジクロロエタン | 0.127 | ジクロロメタン | 0.042 |
| ニトロベンゼン | 0.589 | 水 | 0.123 | トルエン | 0.040 |
| 1-ブタノール | 0.571 | クロロベンゼン | 0.101 | ヘキサン | 0.020 |
表1: マイクロ波電界での加熱効率(tan δ)による一般的な有機溶媒の分類.[1]
一般に,マイクロ波照射と物質との相互作用は,吸収,透過,反射という3つの異なるプロセスによって特徴づけられます(図5). 極性有機溶媒のような誘電性の高い物質では,マイクロ波の吸収性が高いため,媒体が急速に発熱しますが,無極性(マイクロ波透過性)の物質では,マイクロ波との相互作用(伝送)がわずかしかありません. マイクロ波はこのような材料を通過します. そのため,原子炉の建築資材に適しています. マイクロ波が資材の表面で反射すると,システム内にはほぼエネルギーが入りません.

家庭用電子レンジと専用装置の比較
マイクロ波合成の黎明期には,家庭用の電子レンジが化学研究室で広く使われていました. 現在では専用の装置がありますが,今でも台所の電子レンジを科学的な目的で使用する化学者がいます.しかし,専用装置が望ましいという科学的及び実用的な理由から,家庭用電子レンジを加熱源として記述した原稿は,ほぼすべての主要な科学雑誌で受理されなくなっています.[6]
安全性
家庭用電子レンジは,あくまでも家庭用として開発されたものです. したがって,こうした電子レンジには,化学合成のためのアクティブセーフティ機能が備わっていません. それにもかかわらず化学反応に使用した場合,予期しない反応挙動が起きたときに化学者を保護することができません.
測定装置メーカーにとっては,ユーザーに最高の安全性を提供することが最優先事項であるため,専用装置には,極端な温度や圧力条件でも安全に処理できるように,多くの安全機能が実装されています. 300 °Cや80 barでも,安全な処理を保証します.
過熱の可能性
マイクロ波合成では,密閉容器内での溶媒の過熱が重要な利点であり,アレニウスの法則により,反応時間を大幅に短縮することができます.
開放容器システムの場合,時間短縮の可能性は限られています. したがって,密閉容器によるマイクロ波合成では,はるかに広い範囲にアクセスが可能で,使用する溶媒の沸点をはるかに超える温度を適用することができます. 専用のマイクロ波リアクターは,実験プロセス全体を通して反応容器を完全に密閉しておくことができるので,反応混合物を迅速かつ効率的に300 °C,80 barまで加熱できる非常に便利なオートクレーブとして機能します.
優れたパラメーター制御
家庭用の電子レンジは,食品を食べられる温度まで加熱するだけで,反応パラメーターの制御は必要ありません. したがって,家庭用電子レンジでは,反応混合物の温度を測定することはできません. しかし,化学合成では,この温度が重要なパラメーターとなります.
家庭用電子レンジとは対照的に,専用のマイクロ波リアクターには通常,反応温度制御用のIRセンサー,密閉容器内の反応圧力を監視する圧力センサー,適切な攪拌を可能にするマグネチックスターラーが装備されています. また,反応温度をより正確に内部で測定するために,オプションで液浸型温度プローブが用意されていることもあります. 図7は,典型的なマイクロ波実験の加熱プロファイルの例を示しています.この実験では,実験プロセス全体を通してパラメーターが正確に測定,記録されています.

自動化とパラレル合成
時間はお金に等しいため,経済効率を向上させるツールは常に高く評価されています. マイクロ波加熱から得られる大きな利点に加えて,専用のマイクロ波リアクターは,家庭用の電子レンジとは対照的に,ラボのワークフローに対して次の価値あるアプローチを適用できるため,さらなる効率向上が可能です.
- 自動逐次処理では,マイクロ波リアクターと互換性のあるオートサンプラーユニットを使用することで,全自動で夜間に反応を逐次的に処理することができます.
- 反応の並行実施では,1回のマイクロ波実験で最大約200の反応を処理することができます.
ハイスループットの反応スクリーニングから並行スケールアップまでの並行手法と,自動サンプリングユニットの経済的な利点を活用することは,今日では十分に確立された方法です. 家庭用電子レンジでは,このような技術を便利かつ効率的な方法で提供することはできません.
攪拌
家庭用電子レンジとは対照的に,専用のマイクロ波リアクターにはマグネチックスターラーが内蔵されています.適切な攪拌が行われないと,反応混合物内の温度分布が均一にならず,図8に示すとおり,測定温度が温度センサーの位置に依存してしまうため,この点は非常に重要です.

その結果,完全に均質な溶液であっても,効率的な攪拌が保証されずに温度勾配が生じる可能性があるため,マイクロ波加熱の際には攪拌する必要があります. 無溶媒または乾燥媒体の反応や,非常に粘性の高いまたは二相性の反応混合物で,標準的な磁気攪拌が有効でない場合は,十分な混合を保証できないことから,適切な反応温度の決定に細心の注意が必要です.
連続出力
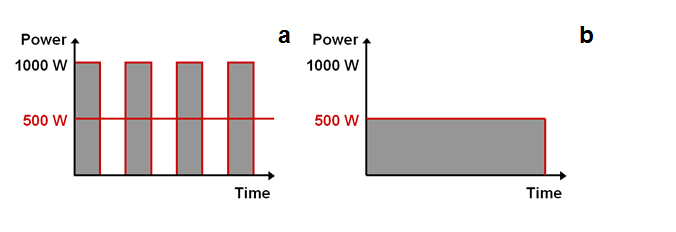
家庭用の電子レンジでは通常,加熱にパルス照射モードを採用しています. 例えば500 Wに設定すると,1000 Wの出力ピークがパルス状に照射され,平均で500 Wが印加されることになります(図8a). このような加熱方法は,家庭で使用する分には十分です. しかし,化学合成では,こうした出力ピークによりホットスポットや制御不能な熱暴走のリスクが生じるため,非常に危険です.
ホットスポットの発生を抑え,熱暴走のリスクを最小限に抑えるために,専用リアクターは連続的な出力を行っています(図8b). これにより,設定した反応温度への到達またはその保持に必要なマイクロ波出力を正確に印加することができます.
ソフトウェア制御
科学的にも経済的にも重要な利点に加えて,専用装置は取り扱いやプログラミングの面でも利点があります. 専用装置は通常,タッチスクリーンで操作する直感的なユーザーインターフェースを備えており,ソフトウェアは実行中の実験の画面上でのモニタリングや編集,データの自動記録,装置やPC上でのデータ管理をサポートしています.
マイクロ波合成の応用領域
従来の合成法のボトルネックとなっていたのは、最適化のステップ、すなわち、目的の生成物を良好な収率と純度で得るために特定の反応の最適条件を見つけることでした。多くの合成反応は、長時間にわたって1つ以上の加熱ステップを必要とするため、こうした最適化はしばしば困難で時間のかかるものでした。条件を制御してマイクロ波で加熱する手法は、反応時間が劇的に短縮されることが多いため(一般的には数日または数時間から数分または数秒にまで短縮)、反応混合物の加熱を必要とするあらゆる用途において価値ある手法であることが示されています。この手法を使えば、並行して、あるいは(自動的に)連続して、化合物を迅速に合成することができます。
複数のバリエーションの反応条件を迅速に実行できるため、朝の「何を試すべきか」という議論が、昼食後には「結果はどうだったか」という議論になります。当然のことながら、ほとんどの製薬会社、農薬会社、バイオテクノロジー会社、マテリアルサイエンス会社は、化学研究室の主要な手法として、すでにマイクロ波合成を多用しています。こうした企業は、マイクロ波技術には化学反応を加速させ、そして生産プロセス全体を加速させる能力があることを理解しています。[7]
以下では、マイクロ波が有効であることが証明されている合成アプリケーションを紹介します。
- 金属触媒による結合形成反応
- Nヘテロ環の合成
- OおよびSヘテロ環の合成
- 炭素環と転位
- スカフォールド デコレーション
- 触媒、配位子、錯体の合成
- 酸化
- ナノマテリアル
- グラフェンとカーボンナノ粒子
- 電池研究用ナノマテリアル
- チタニア、亜鉛、鉄、各種金属酸化物
- カルコゲード
- 金属、ナノ合金
- ゼオライト、モレキュラーシーブ
- 量子ドット
- 金属有機構造体
- 高分子化学
- イオン液体の合成とイオン液体を用いた合成
- 水、亜臨界水、超臨界流体での反応
- バイオディーゼル/バイオマス関連のアプリケーション
- 脱乳化と原油関連反応
- マイクロ波とフローケミストリーの比較
- マイクロ波効果の研究
参考文献
- Leadbeater, N. (2004). Chemistry World, 1, 38
-
Adam, D. (2003). Nature, 421, 571
-
Marx, V. (2004). Chem. & Eng. News, 82, 14;
-
Yarnell, A. (2007). Chem. & Eng. News, 85, 32.
-
Gedye R. et al. (1986). Tetrahedron Lett., 27, 279;
-
Giguere, R. J. et al. (1986). Tetrahedron Lett., 27, 4945.
-
Kappe, C. O., Stadler, A., Dallinger, D. (2012). Microwaves in Organic and Medicinal Chemistry, 2nd Edition. Wiley-VCH, Weinheim.
-
SciFinder scholar search (keyword search: “microwave”) for seven selected synthetic organic chemistry journals: J. Org. Chem., Org. Lett., Tetrahedron, Tetrahedron Lett., Synth. Commun., Synthesis, Synlett.
-
SciFinder scholar search (full text search: “microwave”) for approx. 50 journals. Data for recent years are not available but are estimated to be far higher than for 2008 (in the range of approx. 1000 to 1200 publications per year).
-
J. Org. Chem. 2015, Author Guidelines.
-
Neas, E., Collins, M. (1988). Introduction to Microwave Sample Preparation: Theory and Practice (Eds.: Kingston, H. M., Jassie, L. B.), American Chemical Society, Washington, DC.
-
Herrero, M. A., Kremsner, J. M., Kappe, C. O. (2008). J. Org. Chem., 73, 36.
参考文献
マイクロ波合成の論文
以下は過去10年間のマイクロ波合成に関する科学論文の一覧です。
Microwave-assisted metal-catalyzed reactions
- P. K. Singh et al. 2018. “Aminopyrimidine class aggregation inhibitor effectively blocks Aβ-fibrinogen interaction and Aβ-induced contact system activation,” Biochemistry, 57: 1399.
- Metallosurfactant based Pd-Ni Alloy Nanoparticles as proficient catalyst in Mizoroki Heck Coupling Reaction, N. Kaur et al., Green Chem. 2018, 20, 1506.
- Complex Polycycles from Simple Propargyl Alcohols through Ruthenium-Catalyzed Cascade Reactions and One-Pot Procedures, E. Jäckel et al., Synthesis 2018, 50, 742.
- Divergent synthesis of 1,2-benzo[e]thiazine and benzo[d]thiazole analogs containing a S-trifluoromethyl sulfoximine group. Preparation and new properties of the Adachi reagent, A.-L. Barthelemy et al., J. Org. Chem. 2019, 84, 4086.
Microwave-assisted synthesis of N-heterocycles
- Microwave-assisted one-pot synthesis of new phenanthrene fused-tetrahydrodibenzo-acridinones as potential cytotoxic and apoptosis inducing agents, N. P. Kumar et al., Eur. J. Med. Chem. 2018, 151, 173.
- Copper complexes bearing C-scorpionate ligands: Synthesis, characterization and catalytic activity for azide-alkyne cycloaddition in aqueous medium, A. G. Mahmoud et al., Inorg. Chim. Acta 2018, 483, 371.
- Organocatalytic aza-Michael Reaction to 3-Vinyl-1,2,4-Triazines as a Valuable Bifunctional Platform,
- F. Buttard et al., J. Org. Chem. 2019, 84, 3702.
- Telescoped synthesis of C3-functionalized (E)-arylamidines using Ugi–Mumm and regiospecific quinazolinone rearrangements, V. A. Jaffett et al., Org. Biomol. Chem. 2019, 17, 3118.
- Aziridination and aza-Wharton Reactions of Levoglucosenone, E. T. Ledingham et al., Aust. J. Chem. 2019, 72, 362.
Microwave-assisted synthesis of O- and S-heterocycles
- Microwave-assisted synthesis of novel benzodifuran-based bis(N-(het)arylthiazol-2-amine) derivatives and their antibacterial and antimycobacterial activities, N. H. K. Baba et al., Chem. Heterocycl. Comp. 2018, 54, 658.
- Structure-activity relationship of anticancer potential of 4-hydroxycoumarin and its derivatives:
A comparative study, S. M. Banday et al., Asian J. Pharm. Pharmacol. 2019, 5, 470.
Microwave-assisted rearrangements
- Synthetic and Mechanistic Study on the Microwave Assisted Fries Rearrangement of 1-Methylidene-3,4-dihydroisoquinoline-2(1H)-yl-methanones, F. Haraszti et al., Curr. Org. Chem. 2018, 22, 912.
- Montmorillonite K10-Catalyzed Solvent-Free Conversion of Furfural into Cyclopentenones, S. Bonacci et al., Catalysts 2019, 9, 301.
Microwave-assisted scaffold decoration
- Base-controlled regioselective functionalization of chloro-substituted quinolines, V. E. Murie et al., J. Org. Chem. 2018, 83, 871.
- Pyrrolomycins as antimicrobial agents. Microwave-assisted organic synthesis and insights into their antimicrobial mechanism of action, M. V. Raimondi et al., Bioorg. Med. Chem. 2019, 27, 721.
- On the synthesis, optical and computational studies of novel BODIPY-based phosphoramidate fluorescent dyes, L. A. Machado et al., J. Fluorine Chem. 2019, 220, 9.
Microwave-assisted catalysts, ligands & complexes
- Multifunctional Cyclopentadiene as a Scaffold for Combinatorial Bioorganometallics in
[(η5‐C5H2R1R2R3)M(CO)3] (M = Re, 99mTc) Piano‐stool Type Complexes, A. Frei et al., Chem. Eur. J. 2018, 24, 10153. - Whole Microwave Syntheses of Pyridylpyrazole and of Re and Ru Luminescent Pyridylpyrazole Complexes, B. Merillas et al., Inorg. Chim. Acta 2019, 484, 1.
- Tuning the Luminescent Properties of Ruthenium(II) Amino‐1,10‐Phenanthroline Complexes by Varying the Position of the Amino Group on the Heterocycle, A. S. Abel et al., ChemPlusChem 2019, 84, 498.
Microwave-assisted oxidations
- Copper(II) complexes with an arylhydrazone of methyl 2-cyanoacetate as effective catalysts in the microwave-assisted oxidation of cyclohexane, R. Jlassi et al., Inorg. Chim. Acta 2018, 471, 658.
- Synergistic catalytic action of vanadia–titania composites towards the microwave-assisted benzoin oxidation, F. Ferretti et al., Dalton Trans. 2019, 48, 3198.
Various microwave-assisted organic transformations
- Tropylium-promoted Carbonyl-Olefin Metathesis Reactions, U. P. N. Tran et al., Chem. Sci. 2018, 9, 5145.
- Hydrogen-Bonding-Assisted Ketimine Formation of Benzophenone Derivatives, M.-S. Seo et al., J. Org. Chem. 2018, 83, 14300.
- Efficient Semi-Synthesis of Natural δ-(R)-Tocotrienols from a Renewable Vegetal Source, A. Ville et al., J. Nat. Prod. 2019, 82, 51.
- A New Alternative Synthesis of Salicylaldazine via Microwave Irradiation Method, K. et al., J. Chem. 2019, 9546373.
Microwave-assisted synthesis of nanomaterials
- Simultaneous desulfuration and denitrogenation of model diesel fuel by FeMn microwave modified activated carbon: Iron crystalline habit influence on adsorption capacity, J. A. Arcibar-Orozco et al., J. Clean. Prod. 2019, 218, 69.
- Structural Impact of Zn-insertion into Monoclinic V2(PO4)3: Implications for Zn-ion Batteries, M. J. Park et al., J. Mater. Chem. A 2019, 7, 7159.
- Glyme-Based Electrolyte for Na/Bilayered V2O5 Batteries, X. Liu et al., ACS Appl. Energy Mater. 2019, 2, 2786.
- Self-assembly of hybrid nanorods for enhanced volumetric performance of nanoparticles in Li-ion batteries, M. H. Modarres et al., Nano Lett. 2019,19, 228.
- Nanostructuring of 1-butyl-4-methylpyridinium chloride in ionic liquid–iron oxide nanofluids, A. Joseph et al., J. Therm. Anal. Calorim. 2019, 135, 1373.
- Synthesis of iron oxide nanorods for enhanced magnetic hyperthermia, A. Nikitin et al.,
J. Magn. Magn. Mater. 2019, 469, 443. - Hydrothermal microwave synthesis of SnO microspheres with excellent photocatalytic activity, D. Han et al., Ceram. Int. 2019, 45, 4089.
- Effect of Deposition Time on the Optoelectronics Properties of PbS Thin Films Obtained by Microwave-Assisted Chemical Bath Deposition, E. Barrios-Salgado et al., Adv. Cond. Matter Phys. 2019, 5960587.
- In Situ Microwave‐Assisted Fabrication of Hierarchically Arranged Metal Sulfide Counter Electrodes
to Boost Stability and Efficiency of Quantum Dot‐Sensitized Solar Cells, J.‐S. Tsai et al., Adv. Mater. Interf. 2019, 6, 1801745. - Microwave assisted κ-carrageenan capped silver nanocomposites for eradication of bacterial biofilms,
A. Goel et al., Carbohyd. Polym. 2019, 206, 854. - Microwave-green synthesis of AlPO-n and SAPO-n (n= 5 and 18) nanosized crystals and their assembly in layers, E.-P.Ng et al., Micropor. Mesopor. Mater. 2019, 280, 256.
- XANES, EXAFS, EPR and First Principles Modeling on Electronic Structure and Ferromagnetism in Mn Doped SnO2 Quantum Dots, D. Manikandan et al., J. Phys. Chem. C 2019, 123, 3067.
- Synthesis and characterization of Polymer/Silica/QDs fluorescent nanocomposites with potential application as printing toner, M. Ruiz-Robles et al., Mater. Res. Express 2019, 6, 25314.
- Microwave-Assisted Hydrothermal Synthesis of Agglomerated Spherical Zirconium Phosphate for Removal of Cs+ and Sr2+ Ions from Aqueous System, A. Bashir et al., Applic. Ion Exchange Mater. Environ. 2019, 95.
- A co-operative endeavor by nitrifying bacteria Nitrosomonas and Zirconium based Metal Organic Framework to remove hexavalent chromium, T. Sathvika et al., Chem. Eng. J. 2019, 360, 879.
Microwave-assisted polymer chemistry
- Exfoliation, reduction, hybridization and polymerization mechanisms in one-step microwave-assist synthesis of nanocomposite nylon-6/graphene, P. González-Morones et al., Polymer 2018, 146, 73.
- Synthesis, characterization and chemical degradation of poly(ester-triazole)s derived from D-galactose, M. V. Rivas et al., RSC Adv. 2019, 9, 9860.
- Microwave-assisted esterification step of poly(ethylene terephthalate) (PET) synthesis through ethylene glycol and terephthalic acid, A. C. Espinosa-López et al., Polym. Bull. 2019, 76, 2931.
Microwave-assisted synthesis of and with ionic liquids
- Imidazolium based Ionic liquids as efficient reagents for lignin C-O bond cleavage, M. Thierry et al., ChemSusChem 2018, 11, 439.
- New poly(ionic liquid)s based on poly(azomethine-pyridinium) salts and its use as heterogeneous catalysts for CO2 conversion, E. M. Maya et al., Eur. Polym. J. 2019, 110, 107.
Microwave-assisted biodiesel- and biomass-related applications
- Conversion of sunflower stalk based cellulose to the valuable products using choline chloride based deep eutectic solvents, M. Sert et al., Renew. Energy 2018, 118, 993.
- A synergetic effect of ionic liquid and microwave irradiation on the acid-catalyzed direct conversion of cellulose into methyl glucopyranoside, M. Saito et al., Holzforschung 2018, 72, 1025.
- Microwave assisted biodiesel production using a novel Brønsted acid catalyst based on nanomagnetic biocomposite, S. Chellappan et al., Fuel 2019, 246, 268.
マイクロ波を用いたマイクロ波効果の研究
- Specific microwave effect on Sn- and Ti-MFI zeolite synthesis, Z. Sun et al., RSC Adv. 2017, 7, 35252.
- Microwave effects in the dilute acid hydrolysis of cellulose to 5-hydroxymethylfurfural, N. Sweygers,
et al., Nat. Sci. Rep. 2018, 8, 7719. - Synthesis of Highly Uniform Nickel Multipods with Tunable Aspect Ratio by Microwave Power Control,
P. N. Vakil et al., ACS Nano 2018, 12, 6784.
マイクロ波合成に関する推奨ガイドブック
この20年間、マイクロ波合成に関するさまざまなガイドブックが出版されています。包括的な背景情報を得るための推奨書籍のリストは以下をご覧ください。

マイクロ波合成の無料ガイド
お客様は経験豊富なマイクロ波化学者ですか?それともマイクロ波合成の分野では全くの初心者ですか?
『A Chemist's Guide to Microwave Synthesis(英語版)』が、お客様のステップアップをサポートします。
- Advances in Microwave Chemistry, B. K. Banik, D. Bandyopadhyay (Eds.), 2018, CRC Press, Taylor & Francis Group, Boca Raton
- A Chemist’s Guide to Microwave Synthesis, Volume 3, J. M. Kremsner, A. Stadler, 2018, Anton Paar Publishing, Austria
- Solid-Phase Organic Syntheses, Volume 3: Microwave-Assisted Solid-Phase Organic Synthesis, P. J. H. Scott (Ed.), 2017, Wiley-VCH, Weinheim
- Advances in Microwave Chemistry, B. K. Banik, D. Bandyopadhyay (Eds.), 2018, CRC Press, Taylor & Francis Group, Boca Raton
- Solid-Phase Organic Syntheses, Volume 3: Microwave-Assisted Solid-Phase Organic Synthesis, P. J. H. Scott (Ed.), 2017, Wiley-VCH, Weinheim
- Microwave-assisted Polymer Chemistry, R. Hoogenboom, U. S. Schubert, F. Wiesbrock (Eds.), 2016, Springer, Berlin
- Milestones in Microwave Chemistry, G. Keglevich (Ed.), 2016, Springer, Berlin
- Microwaves in Catalysis: Methodology and Applications, S. Horikoshi, N. Serpone, 2015, Wiley-VCH, Weinheim
- Microwave-assisted Polymerization, A. Mishra, T. Vats, J. H. Clark, 2015, Royal Society of Chemistry, London
- Microwave-Assisted Synthesis of Heterocycles, E. van der Eycken, C. O. Kappe, 2014, Springer, Berlin
- Microwave-Assisted Organic Synthesis: A Green Chemistry Approach, S. C. Ameta, P. B. Punjabi, R. Ameta, C. Ameta (Eds.), 2014, Apple Academic Press, Waretown
- Microwaves in Drug Discovery and Development: Recent Advances, J. Spencer, M. C. Bagley (Eds.), 2014, Future Science Group, London
- Microwaves in Nanoparticle Synthesis: Fundamentals and Applications, S. Horikoshi, N. Serpone, 2013, Wiley-VCH, Weinheim
- Microwaves in Organic and Medicinal Chemistry, C. O. Kappe, D. Dallinger, A. Stadler, 2nd edition, 2012, Wiley-VCH, Weinheim
- Microwaves in Organic Synthesis, A. De La Hoz, A. Loupy (Eds.), 3rd edition, 2012, Wiley-VCH, Weinheim
- Microwave-assisted Cycloaddition Reactions, D. Margetic, 2011, Nova Science Publishers, Hauppauge
- Aqueous Microwave-assisted Chemistry, V. Polshettiwar, R. S. Varma (Eds.), 2010, RSC Publishing, Cambridge
- Practical Microwave Synthesis for Organic Chemists, C. O. Kappe, D. Dallinger, S. S. Murphree, 2009, Wiley-VCH, Weinheim
- Microwave-assisted Proteomics, J. R. Lill, 2009, RSC Publishing, Cambridge
- Microwave-assisted Synthesis of Heterocycles, E. van der Eycken, C. O. Kappe (Eds.), 2006, Springer, Berlin
- Microwave methods in Organic Synthesis, M. Larhed, K. Olofsson (Eds.), 2006, Springer, Berlin
- Microwave-assisted Organic Synthesis: 100 reaction procedures, D. Bogdal, 2005, Elsevier, Amsterdam
- Microwave-assisted Organic Synthesis, J. P. Tierney, P. Lidström (Eds.), 2005, Blackwell, Oxford